국방품질연구회(DQS)가 전하는 품질 인사이트
DQS 매거진
탄약 추진제의 노화특성 및 수명예측 모델 소개
2024. 02. 26
국방기술품질원 이화학시험분석팀 배만재 책임연구원

국방기술품질원 이화학시험분석팀 천보하 연구원

탄약 추진제의 신뢰성 평가는 저장 기간에 따른 추진제의 자연분해로 감소 되는 안정제 함량을 분석하여 결정하는 것이 가장 상용화된 방법이며, 선진국에서는 안정제 감량, 열 발생, 산화질소 발생 및 무게 감량 등의 다양한 방법으로 분석하고 있다. 따라서, 다양한 안정제 함량 시험규격들을 조사하여 평가 요소별로 구분하여 4개의 카테고리로 분류하였다.
추가로, 추진제의 저장수명 예측에 사용되는 시간에 따른 안정제 함량 감소를 추정하기 위한 수명예측 모델을 소개하고자 한다.
서론
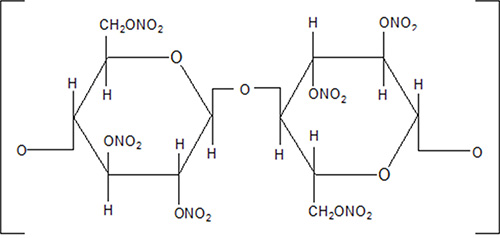
일반적인 탄약 추진제의 주요 성분은 Nitro cellulose(NC)이며, NC는 그림1과 같이 -R-ONO2기를 포함한 질산에스테르 화합물로서 장시간 저장하면 수분, 직사광선, 열, 산성 물질에 의해 분해되어, 질소산화물(NOx)과 질산(HNO3)을 생성한다. NC의 자연분해 생성물들이 질산에스테르 분해를 촉진하는 열분해(Thermolysis) 및 가수분해(Hydrolysis)로 자동촉매반응(Auto Catalysis Reaction)을 유도하여 다시 추진제의 온도를 상승시키면서 연소온도 이상에 도달하게 되면 자연발화가 일어나게 된다.
NC의 분해로 발생 되는 추진제의 자연 분해를 근본적으로 방지할 수는 없으나, 분해 생성물에 의한 자동촉매반응의 유도를 억제하면 분해반응의 가속을 지연시킬 수 있다. NC의 분해반응 생성물인 질소산화물과 먼저 반응하여, 질소산화물을 제거하기 위하여 추진제 제조 시 염기성의 안정제(DPA, Diphenylamine)를 소량 첨가(대략 1.0%)하고 있다.
요약하면, 안정제는 NC보다 질소산화물과 훨씬 친화력 있어 질소산화물이 NC와 반응하기 전에 안정제와 반응하게 되고, 장기 저장에 따라 안정제 함량은 감소하며, 질소화합물과 반응하여 생성되는 유도체함량은 증가하게 된다. 따라서, 국방기술품질원에서 수행 중인 추진제의 신뢰성 평가는 안정제의 함량을 기준으로 수행하고 있다.
추진제
단기추진제의 주요성분인 NC는 질산에스테르 화합물로서 장기 저장 시 환경요인(수분, 직사광선, 열, 산성물질 등)에 의해, 열분해 및 가수분해인 자연분해 현상이 발생하기 쉽다.
열분해
NC는 질산에스테르 화합물로 질산에스테르 결합이 유리되어, 자유라디칼 RO · 와 NO2 · 로 분해된다
(NC) RO-NO2 → RO · + NO2 ·
추진제 내의 NC 및 다른 유기물과 반응하여 더 많은 질소산화물과 CO, CO2, H2O 등을 발생시킨다. 이때 추진제의 온도는 더욱 상승하고 심한 경우 연소온도 이상에 도달하게 되면 추진제의 자연발화가 일어나게 된다.
NO2 · + NC → NO
NO + O2 → NO2 ·
2CH2O + 3NO2 → 3NO + 2H2O + CO + CO2
3CH2 + 7NO2 → 7NO + 3H2O + 2CO + CO2
RO · + NO → RONO
가수분해
질산에스테르 화합물은 장기저장하면 추진제 주위의 수분 또는 습기와 반응하여 ROH + H+ + NO3-로 분해 된다.
(NC) RO-NO2 → ROH + H+ + NO3-
H+와 NO3-는 서로 반응하여 질산을 생성시키고, 생성된 H+는 추진제 내의 NC와 지속적으로 반응하여 NC를 분해시키고, NO3-는 연쇄반응을 통하여 질소산화물과 질산을 생성시킨다. 이 때 발생한 온도의 증가는 추진제의 열분해 반응으로 이어져 분해 반응을 더욱 촉진시킨다.
R'NO2 + H+ → R'OH + NO2+
NO2+ + NO3- → N2O5
N2O5 + H2O → 2HNO3 ↔ 2H+ + 2NO3-
안정제
DPA 안정제
단기추진제에 주로 사용되는 유기안정제인 DPA는 약염기성 물질로 NC의 자연분해를 근본적으로 방지할 수는 없으나 NC내 불순물의 분해, 잔류 용매의 산화 또는 NC의 자연분해로 생성되는 산생성물(Acid product)을 중화시키기에는 충분한 것으로 알려져 있다. DPA의 물리적 특성은 표1과 같다. DPA 함량은 1.0∼2.5%의 범위에서 가장 좋은 효과를 얻을 수 있으며 5%를 초과하면 DPA의 기본 성질이 추진제에 해로운 영향을 끼치는 것으로 알려져 있다.
| Classification | Properties |
|---|---|
| Molecular formula | C12H11N |
| Structural formula |
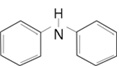
|
| Nitrogen content | 8.28 % |
| Density | 1.16 g/㎤ |
| Color | Colorless |
| Melting point | 54 ℃ |
| Boiling point | 302 ℃ |
| Solubility |
Benzene : Insoluble her-alcohol : Soluble |
표 1. DPA 물리적 특성
안정제 분해
추진제에 포함되는 안정제는 염기성인 DPA(Diphenylamine)가 사용된다. DPA 분자는 NC에서 분해되는 6분자의 질소산화물과 반응할 수 있어 효과적으로 추진장약의 자연분해 반응을 억제할 수 있는데 이러한 반응이 질소산화물의 결합 위치와 결합 개수에 따라서 다양한 유도체를 생성할 수 있다.
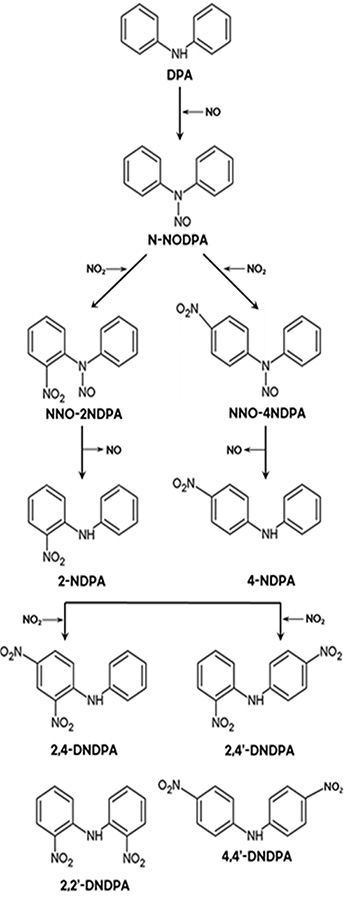
안정제(DPA)의 예측되는 분해경로는 그림2와 같이 알려져 있다. 저장 중인 추진제(NC)에서 발생하는 NO와 결합한 DPA는 N-nitrosation 반응으로 N-NODPA (N-nitroso diphenylamine)로 우선 분해되고, 이후 NO2 기체에 의한 C-nitration 반응을 통해 생성되는 mono-nitro-DPA 유도체 그룹인 2-NDPA(2-nitrodiphenyl amine), 4-NDPA (4-nitrodiphenyl amine), 그리고 마지막 유효 안정제 그룹은 mono-nitro-DPA 유도체가 NO2 기체에 의한 nitration 반응을 통해서 형성된 4개 dinitro-유도체인 2,4-DNDPA (2,4-dinitrodiphenylamine), 2,4'-DNDPA(2,4'-dinitrodiphenyl amine), 2,2’-DNDPA(2,2'-dinitrodiphe nyl amine), 4,4’-DNDPA(4,4'-dinitro diphenylamine)으로 분해되는 것으로 예상할 수 있다.
추진제 노화에 따른 DPA 질화 공정(Nitration process)에 대한 문헌들을 조사한 결과, 니트로화 DPA 유도체는 주로 N-NODPA, 소량의 mononitro-DPA 및 dinitro-DPA를 형성하는 분해반응을 통해 생성된다. 이론적으로 trinitro-, tetranitro- 및 hexanitro- 유도체를 얻을 수 있지만, 실질적으로는 강제 분해 공정에서만 관찰되고 있다. 또한, 선행 연구결과에 의하면 유도체 중 2개 이하의 질소산화물과 결합한 중간유도체는 추진제의 분해반응을 억제하는 유효한 안정제로 역할을 하며, 이보다 많은 질소산화물과 결합된 유도체는 안정제의 역할은 하지만 그 효과는 미미한 것으로 보고하고 있다.
추진제 안전성 평가
추진제의 안전성을 위한 평가는 단일온도에서 수행되며, 다양한 방법들이 규격화되어 있다. 안정제 함량을 분석하는 방법은 MIL-STD-286C에 명시되어 있으며, 안정제 함량을 중량으로 측정하는 방법으로 추진제에서 안정제를 분리하여, HPLC 또는 UV-Vis 장비를 이용하여 기준치에 합부 여부를 판정한다. 열에너지의 흐름인 열류(Heat flow)를 측정하는 방법은 설정된 온도와 시간을 기준으로 열류를 HFC(Heat flow calorimeter) 장비를 이용하여 측정하고 적용규격은 나토(NATO) 국방표준국에서 작성한 표준규격서인 STANAG 4582이다. 가속노화시험으로는 MIL-STD-286C에 따라 설정된 온도와 시간에 따라 질소산화물(NOx)이 생성되는 시간을 특정하며 육안으로 적색 연기를 확인하는 방법과 MVP(Methyl violet paper)의 색상변화를 확인하는 방법이 있다. 또한 나토(NATO) 국방표준국에서 작성한 AOP-7에는 설정된 온도와 시간을 기준으로 Starch-iodide test paper의 변색을 확인을 그림3의 장비를 사용하는 Abel heat test 방법과 설정된 온도와 시간을 기준으로 생성된 질소산화물(NOx) 가스를 중화적정하여 정량을 확인하는 Bergmann -junk test 방법이 있다.

STANAG 4556에서는 정해진 온도와 시간을 기준으로 진공조건에서 발생된 가스의 부피를 특정하는 Vacuum stability test를 규정하고 있다. 이외에 독일에서는 90℃와 105℃에서 일정 시간동안 노화 후에 무게 감량을 측정하는 Weight loss test를 사용하는 것으로 알려져 있다. 이런 다양한 시험방법들을 평가요소별도 분류하면 표2와 같다.
| 평가 요소 | 시험 내용 | 시험 규격 |
|---|---|---|
| 안정제 감량 | 안정제 함량분석 (HPLC/ UV-Vis) | MIL-STD-286C (217.5/ 201.4.2) |
| 열 발생 | HFC 노화시험 (60∼90℃) | STANAG 4582 |
| NOx발생 | Surveillance Test (65.5℃) / Heat Test (120 / 134.5℃) | MIL-STD-286C (407.1/404.1.2) |
| Abel Test / Bergmann-junk Test | AOP-7 (202.02.004/202.01.004) | |
| Vacuum Stability Test(90 / 100℃) | STANAG 4556 MIL-STD-286C(403.1.3) | |
| 무게 감량 | 가속노화/Weight Loss(95 / 105℃) | AOP-7 (202.01.001) |
표 1. DPA 물리적 특성
추진제 수명예측 모델
안정제 함량 변화 모델은 STANAG 4527에 명시된 0차 또는 1차의 반응속도 모델 2가지가 주로 사용되었다. 2008년도에 NC 기반의 추진제의 화학적 안정성과 저장수명을 예측하는 NATO의 새로운 표준인AOP-48이 발행되면서, n차 반응속도 모델이 추가되었다. AOP-48은 다중구간 온도 노화를 통하여 n차 반응속도를 분석하고 반응속도 모델링을 통한 저장수명을 예측할 수 있는 방법을 제시하고 있다.
0차 반응속도 모델
0차 반응속도 모델은 시간에 따라 안정제 함량이 선형으로 감소한다는 가정으로 시작한다. 안정제 함량 변화에 대한 0차 반응속도는 식(1)로 표현 할 수 있다.

식(1)을 변수 분리 후, 적분을 취하면 안정제 함량 변화에 대한 모델은 식(2)로 표현할 수 있다.
식(2)는 1차 방정식으로서 저장시간에 따른 안정제의 함량 변화와 Arrhenius 식을 활용하여 구하고자 하는 온도의 반응속도 상수를 구할 수 있다. 온도의 반응속도 상수를 식(2)에 적용하면, 구하고자 하는 온도의 저장수명을 예측할 수 있다.
1차 반응속도 모델
1차 반응속도 모델은 시간에 따라 안정제 함량의 자연로그 값이 일정하게 감소하여 반응이 진행됨에 따라 안정제 감소 속도가 점차 느려진다는 것을 가정으로 시작한다. 1차 반응속도는 식(3)으로 표현할 수 있다.

식(3)을 변수 분리 후, 적분을 취하면 안정제 함량 변화에 대한 모델은 식(4)로 표현할 수 있다.
상기 식은 지수 방정식으로서 양변에 자연로그를 취하면 식(5)와 같이 1차 방정식 형태가 되므로 최소제곱법을 활용하여 온도별 반응속도 상수를 구할 수 있다.
온도별 반응속도 상수가 구해지면, 0차 반응속도 모델과 동일한 방법으로 Arrhenius 식을 활용하여 구하고자 하는 온도일 때의 반응속도 상수를 구할 수 있고, 1차 방정식인 식(5)를 활용하여 구하고자
n차 반응속도 모델
n차 반응속도 모델은 시간에 따라 안정제 함량 감소 추이가 고유한 패턴으로 진행된다는 가정으로 시작한다. n차 반응속도 식을 활용하면, 최적의 활성화 에너지(Ea), 빈도계수(A) 및 반응차수(n)를 구할 수 있다. n차 반응속도는 식(6)으로 표현할 수 있다.

식(6)을 변수 분리 후, 적분을 취하면 안정제 함량 변화에 대한 모델은 (7)로 표현할 수 있다.
0차 또는 1차 반응속도 모델과는 다르게 안정제의 농도이므로 단위는 무차원이 되며, C 와 C0는 (8)로 표현할 수 있다.
식(8)을 식(7)에 대입하여 정리하면 (9)와 같이 표현할 수 있다.

식(9)의 반응속도 상수인 k에 Arrhenius 식을 대입하여 정리하면, 식(10)과 같다.

식(10)을 시간(t)에 관하여 정리하면 식(11)과 같다.

식(11)에 임의의 값인 반응차수(n)를 넣어주면, 활성화에너지(Ea)와 빈도계수(A)를 구할 수 있다. 최적의 반응차수는 상대적으로 추정표준오차(SEE, Standard Error of Estimate)가 가장 작은 값을 나타내는 반응차수(n)이다. 최적의 반응차수는 Try and Error법으로 산출할 수 있으며, 추정표준오차(SEE)는 식(12)로 표현될 수 있다.



최적의 반응차수(n)를 찾고 나면, 식(11) 에 대입하여 구하고자 하는 온도에 따른 저장수명을 예측할 수 있다. 2015년도에 발표된 논문을 사례로 들면, 4가지 온도(50℃, 60℃, 70℃, 80℃)에서 80일 동안 고온가속노화를 진행하여 2~7일 간격으로 안정제 함량을 측정하였다, 그 값을 바탕으로 반응차수(n)를 0.00001에서 2.40001까지 0.00001 간격으로 n차 반응속도모델에 대입하여 최적의 반응차수를 도출하였고, 활성화에너지(Ea)와 빈도계수(A)를 구하여 속도모델을 완성하였다. 그 후, 완성된 반응속도모델을 이용하여 온도별 저장수명을 예측하여 결과를 발표하였다. 반응속도 모델은 추진제를 일정 온도로 저장하는 것으로 가정하여 저장수명을 예측하므로, 실제 탄약저장고 내부의 일교차와 계절에 따른 온도 분포 등의 요인을 반영할 수 없어 정확한 예측에는 한계가 있다.
맺음말
탄약 추진제의 수명예측은 국방기술품질원에서 수행하는 저장탄약 신뢰성평가 (ASRP)의 안정제 함량 분석주기 선정 이외에 탄약의 보급 및 정비계획 수립, 폐기 시기의 결정 등에 폭넓게 활용될 수 있는 분야이다. 추진제의 열적 스트레스에 대한 저장 안전성을 신뢰성 있게 관리하기 위하여 평가 시점의 안정성을 분석하는 시험 이외에 저장수명을 관리하는 시험을 추가하며, 수명예측 모델을 통한 이론적 결과의 검증을 위하여 평가결과에 대한 Database 관리가 필요한 것으로 판단 된다.
- 참고문헌
-
- 1. Z. Sun, X. Fu, H. Yu, X. Fan, X. Ju, “Theoretical study on stabilization mechanisms of nitrate esters using aromatic amines as stabilizers”, Journal of Hazardous Materials, Vol.339, No.5, pp.401-408, 2017.
- 2. T. Lindblom, “Reaction in stabilizer and between stabilizer and nitrocellulose in propellants”, Propellants, Explosives, Pyrotechnics, Vol.27, pp.197-208, 2002.
- 3. Military Agency for Standardization, “Explosive, chemical stability nitrocellulose based propellants, procedure for assessment of chemical life and temperature dependence of stabilizer consumptions rates,” NATO, STANAG 4527 (Edition 1), 2004
- 4. Military Agency for Standardization, “Explosives, nitrocellulose based propellants – stability test procedures and requirements using stabilizer depletion,” NATO, AOP-48 Ed. 2, 2008
